البلازما الغنية بالصفائح الدموية الحديثة: "البلازما الغنية بالصفائح الدموية السريرية"
في السنوات العشر الماضية، شهد نظام العلاج بالبلازما الغنية بالصفائح الدموية تغييرات كبيرة.ومن خلال الأبحاث التجريبية والسريرية، أصبح لدينا الآن فهم أفضل للصفائح الدموية وفسيولوجيا الخلايا الأخرى.بالإضافة إلى ذلك، أظهرت العديد من التقييمات المنهجية عالية الجودة والتحليلات التلوية والتجارب المعشاة ذات الشواهد فعالية تقنية PRP الحيوية في العديد من المجالات الطبية، بما في ذلك الأمراض الجلدية وجراحة القلب والجراحة التجميلية وجراحة العظام وإدارة الألم وأمراض العمود الفقري والطب الرياضي. .
السمة الحالية لـ PRP هي تركيز الصفائح الدموية المطلق، والذي يتغير من التعريف الأولي لـ PRP (بما في ذلك تركيز الصفائح الدموية أعلى من القيمة الأساسية) إلى أكثر من 1 × 10 6/ميكرولتر أو حوالي 5 أضعاف الحد الأدنى لتركيز الصفائح الدموية في الصفائح الدموية من حدود.في المراجعة الشاملة التي أجراها فادادو وآخرون.تم تقييم 33 نظامًا وبروتوكولًا لـ PRP.يكون عدد الصفائح الدموية في مستحضر PRP النهائي الذي تنتجه بعض هذه الأنظمة أقل من عدد الدم الكامل.وأفادوا أن عامل الصفائح الدموية لـ PRP ارتفع إلى مستوى منخفض يصل إلى 0.52 باستخدام مجموعة الدوران الفردية (Selphyl ®).في المقابل، فإن نظام EmCyte Genesis PurePRPII ® ذو الدوران المزدوج، يعتبر تركيز الصفائح الدموية التي ينتجها الجهاز هو الأعلى (1.6 × 10 6 / ميكرولتر).
من الواضح أن الأساليب المختبرية والحيوانية ليست بيئة بحثية مثالية للتحول الناجح إلى الممارسة السريرية.وبالمثل، فإن دراسة مقارنة الأجهزة لا تدعم القرار، لأنها تظهر أن تركيز الصفائح الدموية بين أجهزة PRP مختلف تمامًا.لحسن الحظ، من خلال التكنولوجيا والتحليلات القائمة على البروتينات، يمكننا زيادة فهمنا لوظائف الخلية في PRP التي تؤثر على نتائج العلاج.قبل التوصل إلى توافق في الآراء بشأن مستحضرات وتركيبات PRP الموحدة، يجب أن يتبع PRP تركيبات PRP السريرية لتعزيز آليات إصلاح الأنسجة الكبيرة والنتائج السريرية التقدمية.
صيغة PRP السريرية
في الوقت الحاضر، تم وصف PRP السريري الفعال (C-PRP) على أنه تركيبة معقدة من مكونات متعددة الخلايا ذاتية المنشأ في بلازما صغيرة الحجم تم الحصول عليها من جزء من الدم المحيطي بعد الطرد المركزي.بعد الطرد المركزي، يمكن استعادة PRP ومكونات الخلايا غير الصفائحية من جهاز التركيز وفقًا لكثافات الخلايا المختلفة (التي تكون كثافة الصفائح الدموية هي الأقل منها).
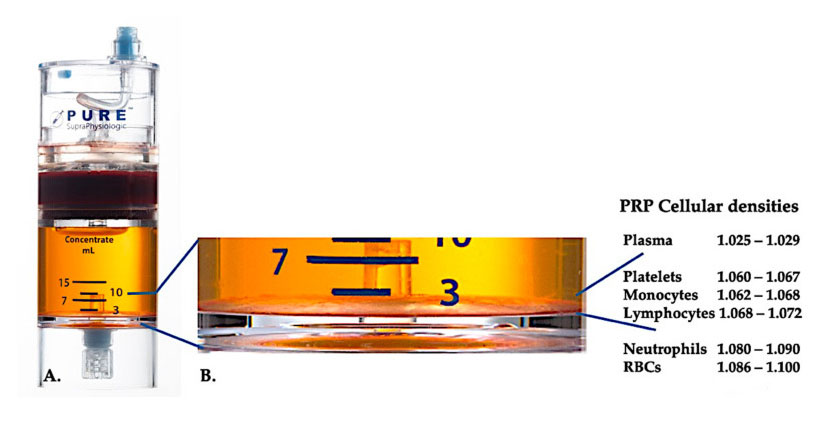
تم استخدام معدات فصل كثافة الخلايا PurePRP-SP ® (EmCyte Corporation، Fort Myers، FL، USA) للدم الكامل بعد إجراءين للطرد المركزي.بعد عملية الطرد المركزي الأولى، تم فصل مكون الدم بالكامل إلى طبقتين أساسيتين، معلق البلازما الصفائح الدموية (العجاف) وطبقة خلايا الدم الحمراء.في A، تم الانتهاء من خطوة الطرد المركزي الثانية.يمكن استخراج حجم PRP الفعلي لتطبيق المريض.يُظهر التكبير في B أن هناك طبقة بنية لترسيب كرات الدم الحمراء متعددة المكونات (ممثلة بالخط الأزرق) في الجزء السفلي من الجهاز، والتي تحتوي على تركيزات عالية من الصفائح الدموية والخلايا الوحيدة والخلايا الليمفاوية، بناءً على تدرج الكثافة.في هذا المثال، وفقًا لبروتوكول إعداد C-PRP مع العدلات الفقيرة، سيتم استخراج الحد الأدنى من النسبة المئوية للعدلات (<0.3%) وكريات الدم الحمراء (<0.1%).
حبيبات الصفائح الدموية
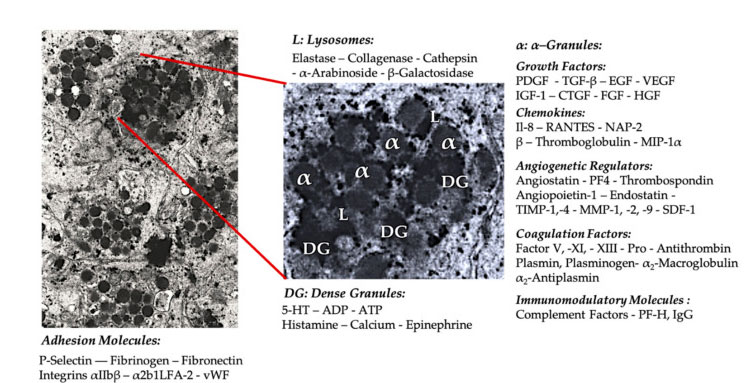
في تطبيق PRP السريري المبكر، تعد حبيبات α هي البنية الداخلية للصفائح الدموية الأكثر شيوعًا، لأنها تحتوي على عوامل تخثر، وعدد كبير من PDGF ومنظمات تكوين الأوعية، ولكن لها وظيفة تجلط الدم قليلة.تشمل العوامل الأخرى مكونات كيموكينية وسيتوكينات أقل شهرة، مثل عامل الصفائح الدموية 4 (PF4)، والبروتين الأساسي قبل الصفائح الدموية، وP-selectin (منشط للإنتجرين) والكيموكين RANTES (يتم تنظيمه عن طريق التنشيط، والتعبير عن الخلايا التائية الطبيعية ويفترض أنها إفراز).تتمثل الوظيفة العامة لمكونات حبيبات الصفائح الدموية المحددة في تجنيد وتنشيط الخلايا المناعية الأخرى أو تحفيز التهاب الخلايا البطانية.
يتم استخدام المكونات الحبيبية الكثيفة مثل ADP والسيروتونين والبولي فوسفات والهستامين والأدرينالين بشكل ضمني كمنظم لتنشيط الصفائح الدموية والتخثر.والأهم من ذلك أن العديد من هذه العناصر لها وظيفة تعديل الخلايا المناعية.يتم التعرف على الصفائح الدموية ADP بواسطة مستقبل P2Y12ADP على الخلايا الجذعية (DC)، وبالتالي زيادة الالتقام الخلوي للمستضد.تعد DC (خلية تقديم المستضد) مهمة جدًا لبدء الاستجابة المناعية للخلايا التائية والتحكم في الاستجابة المناعية الوقائية، التي تربط الجهاز المناعي الفطري والجهاز المناعي التكيفي.بالإضافة إلى ذلك، ترسل الصفائح الدموية أدينوزين ثلاثي الفوسفات (ATP) إشارات عبر مستقبل الخلايا التائية P2X7، مما يؤدي إلى زيادة تمايز الخلايا المساعدة CD4 T إلى خلايا T المساعدة 17 (Th17) المسببة للالتهابات.تحفز مكونات الحبيبات الكثيفة الصفائح الدموية الأخرى (مثل الغلوتامات والسيروتونين) على هجرة الخلايا التائية وزيادة تمايز الخلايا الوحيدة إلى العاصمة، على التوالي.في PRP، يتم إثراء هذه المعدلات المناعية المشتقة من الجسيمات الكثيفة بدرجة عالية ولها وظائف مناعية كبيرة.
عدد التفاعلات المحتملة المباشرة وغير المباشرة بين الصفائح الدموية والخلايا (المستقبلة) الأخرى واسع النطاق.ولذلك، فإن تطبيق PRP في بيئة الأنسجة المرضية المحلية يمكن أن يؤدي إلى مجموعة متنوعة من التأثيرات الالتهابية.
تركيز الصفائح الدموية
يجب أن يحتوي C-PRP على جرعات سريرية من الصفائح الدموية المركزة لإنتاج تأثيرات علاجية مفيدة.يجب أن تحفز الصفائح الدموية الموجودة في C-PRP تكاثر الخلايا، وتوليف العوامل الوسيطة والعوامل العصبية، وتعزز هجرة الخلايا الكيميائية وتحفز نشاط التنظيم المناعي، كما هو موضح في الشكل.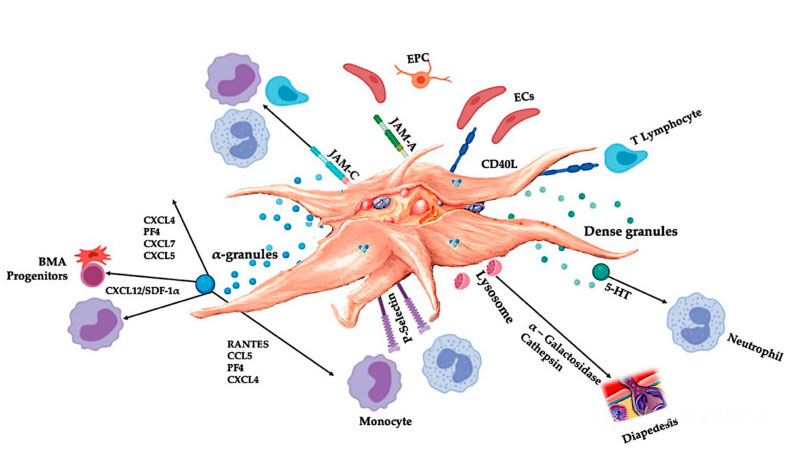
تتوسط الصفائح الدموية المنشطة، وإطلاق PGF وجزيئات الالتصاق، مجموعة متنوعة من التفاعلات الخلوية: الانجذاب الكيميائي، والتصاق الخلايا، والهجرة، وتمايز الخلايا، وتنظيم الأنشطة التنظيمية المناعية.تساهم تفاعلات خلايا الصفائح الدموية هذه في تكوين الأوعية الدموية والنشاط الالتهابي، وفي النهاية تحفز عملية إصلاح الأنسجة.الاختصارات: BMA: نضح نخاع العظم، EPC: الخلايا السلفية البطانية، EC: الخلايا البطانية، 5-HT: 5-هيدروكسيتريبتامين، RANTES: التنظيم المنشط للتعبير الطبيعي للخلايا التائية والإفراز المفترض، JAM: نوع جزيء التصاق الوصلة، CD40L: كتلة 40 يجند، SDF-1 α: عامل مشتق من الخلايا اللحمية -1 α، CXCL: يجند كيموكين (عزر CXC)، PF4: عامل الصفائح الدموية 4. مقتبس من Everts et al.
كان ماركس أول من أثبت تعزيز شفاء العظام والأنسجة الرخوة، وكان الحد الأدنى لعدد الصفائح الدموية 1 × 10 6 / ميكرولتر. وقد تم تأكيد هذه النتائج في دراسة الدمج القطني من خلال الثقبة بين الفقرات، عندما كانت جرعة الصفائح الدموية أكبر من 1.3 × عند 106 صفائح دموية/ميكرولتر، أظهرت هذه الدراسة المزيد من الاندماج.وبالإضافة إلى ذلك، جيوستي وآخرون.تم الكشف عن 1.5 × تتطلب آلية إصلاح الأنسجة بجرعة 109 صفائح دموية / مل للحث على تكوين الأوعية الدموية الوظيفية من خلال نشاط الخلايا البطانية.في الدراسة الأخيرة، أدت التركيزات الأعلى إلى تقليل إمكانية تكوين الأوعية الدموية للصفائح الدموية داخل الجريبات وحولها.بالإضافة إلى ذلك، أظهرت البيانات السابقة أن جرعة البلازما الغنية بالصفائح الدموية ستؤثر أيضًا على نتائج العلاج.لذلك، من أجل تحفيز تفاعل تكوين الأوعية بشكل كبير وتحفيز تكاثر الخلايا وهجرة الخلايا، يجب أن يحتوي C-PRP على 7.5 على الأقل في زجاجة علاج PRP سعة 5 مل × 10 9 يمكنها توصيل الصفائح الدموية.
بالإضافة إلى الاعتماد على الجرعة، يبدو أن تأثير PRP على نشاط الخلية يعتمد بشكل كبير على الوقت.صوفي وآخرون.تشير هذه النتائج إلى أن التعرض قصير المدى للصفائح الدموية البشرية يمكن أن يحفز تكاثر خلايا العظام والانجذاب الكيميائي.على العكس من ذلك، فإن التعرض طويل الأمد للبلازما الغنية بالصفائح الدموية سيؤدي إلى انخفاض مستويات الفوسفاتيز القلوي وتكوين المعادن.
خلية دم حمراء
خلايا الدم الحمراء هي المسؤولة عن نقل الأكسجين إلى الأنسجة ونقل ثاني أكسيد الكربون من الأنسجة إلى الرئتين.ليس لها نواة وتتكون من جزيئات الهيم التي ترتبط بالبروتينات.تعمل مكونات الحديد والهيم في خلايا الدم الحمراء على تعزيز مزيج الأكسجين وثاني أكسيد الكربون.بشكل عام، تبلغ دورة حياة خلايا الدم الحمراء حوالي 120 يومًا.تتم إزالتها من الدورة الدموية بواسطة البلاعم من خلال عملية تسمى شيخوخة كرات الدم الحمراء.قد تتضرر خلايا الدم الحمراء في عينات البلازما الغنية بالصفائح الدموية (PRP) في ظل ظروف القص (على سبيل المثال، جراحة نزيف الدم الكامل، أو العملية المناعية، أو الإجهاد التأكسدي أو عدم كفاية نظام تركيز البلازما الغنية بالصفائح الدموية).لذلك، يتحلل غشاء خلية الدم الحمراء ويطلق الهيموجلوبين السام (Hb)، الذي يتم قياسه بواسطة الهيموجلوبين الحر في البلازما (PFH)، والهيم والحديد.].يؤدي PFH ومنتجات تحلله (الهيم والحديد) معًا إلى تأثيرات ضارة وسمية للخلايا على الأنسجة، مما يؤدي إلى الإجهاد التأكسدي وفقدان أكسيد النيتريك وتنشيط المسارات الالتهابية وكبت المناعة.ستؤدي هذه التأثيرات في النهاية إلى خلل في دوران الأوعية الدقيقة، وتضيق الأوعية المحلية وإصابة الأوعية الدموية، فضلاً عن تلف الأنسجة الخطير.
الشيء الأكثر أهمية هو أنه عندما يتم تسليم كرات الدم الحمراء المحتوية على C-PRP إلى الأنسجة، فسوف يتسبب ذلك في تفاعل موضعي يسمى داء الكريات الحمر، والذي سيؤدي إلى إطلاق مثبط فعال لهجرة السيتوكين والبلاعم.يمنع هذا السيتوكين هجرة الخلايا الوحيدة والبلاعم.إنه يرسل إشارات قوية مؤيدة للالتهابات إلى الأنسجة المحيطة، ويمنع هجرة الخلايا الجذعية وتكاثر الخلايا الليفية، ويؤدي إلى خلل وظيفي كبير في الخلايا المحلية.ولذلك، من المهم الحد من تلوث كرات الدم الحمراء في الاستعدادات للبلازما الغنية بالصفائح الدموية.بالإضافة إلى ذلك، لم يتم تحديد دور خلايا الدم الحمراء في تجديد الأنسجة.عادة ما تؤدي عملية الطرد المركزي والتحضير الكافية لـ C-PRP إلى تقليل أو حتى القضاء على وجود خلايا الدم الحمراء، وبالتالي تجنب العواقب الضارة لانحلال الدم وكثرة الحمر.
الكريات البيض في C-PRP
يعتمد وجود خلايا الدم البيضاء في مستحضرات PRP على معدات العلاج ونظام التحضير.في معدات PRP المعتمدة على البلازما، يتم التخلص تمامًا من خلايا الدم البيضاء؛ومع ذلك، تركزت خلايا الدم البيضاء بشكل ملحوظ في إعداد PRP للطبقة البنية لترسيب كرات الدم الحمراء.نظرًا لآليات الدفاع المناعية والمضيفة، تؤثر خلايا الدم البيضاء بشكل كبير على البيولوجيا الداخلية لحالات الأنسجة الحادة والمزمنة.سيتم مناقشة هذه الميزات أدناه.ولذلك، فإن وجود كريات الدم البيضاء المحددة في C-PRP يمكن أن يسبب تأثيرات خلوية وأنسجة كبيرة.وبشكل أكثر تحديدًا، تستخدم أنظمة الطبقة البنية والأصفر لترسيب كرات الدم الحمراء المختلفة مخططات تحضير مختلفة، وبالتالي تنتج نسبة مختلفة من العدلات والخلايا الليمفاوية والخلايا الأحادية في PRP.لا يمكن قياس الحمضات والقاعدات في مستحضرات PRP لأن أغشية خلاياها هشة للغاية بحيث لا تتحمل قوى المعالجة الطاردة المركزية.
العدلات
العدلات هي كريات الدم البيضاء الأساسية في العديد من مسارات الشفاء.تتحد هذه المسارات مع البروتينات المضادة للميكروبات الموجودة في الصفائح الدموية لتشكل حاجزًا كثيفًا ضد مسببات الأمراض الغازية.يتم تحديد وجود العدلات وفقًا لهدف علاج C-PRP.قد تكون هناك حاجة إلى زيادة مستويات التهاب الأنسجة في العلاج الحيوي بالبلازما الغنية بالصفائح الدموية (PRP) للعناية بالجروح المزمنة أو في التطبيقات التي تهدف إلى نمو العظام أو شفاءها.الأهم من ذلك، تم العثور على وظائف العدلات إضافية في عدة نماذج، مع التركيز على دورها في تكوين الأوعية الدموية وإصلاح الأنسجة.ومع ذلك، يمكن أن تسبب العدلات أيضًا تأثيرات ضارة، لذا فهي غير مناسبة لبعض التطبيقات.أثبت تشو ووانغ أن استخدام PRP الغني بالعدلات يمكن أن يؤدي إلى زيادة نسبة الكولاجين من النوع الثالث إلى الكولاجين من النوع الأول، وبالتالي يؤدي إلى تفاقم التليف وتقليل قوة الأوتار.الخصائص الضارة الأخرى التي تتوسطها العدلات هي إطلاق السيتوكينات الالتهابية والبروتينات المعدنية المصفوفية (MMPs)، والتي يمكن أن تعزز الالتهاب والتقويض عند تطبيقها على الأنسجة.
الكريات البيض
في C-PRP، تكون الخلايا الليمفاوية T وB أحادية النواة أكثر تركيزًا من أي خلايا دم بيضاء أخرى.وهي ترتبط ارتباطًا وثيقًا بالمناعة التكيفية السامة للخلايا.يمكن للخلايا الليمفاوية تحفيز تفاعلات الخلايا لمحاربة العدوى والتكيف مع الغزاة.بالإضافة إلى ذلك، تعمل السيتوكينات المشتقة من الخلايا اللمفاوية التائية (الإنترفيرون γ [IFN- γ] والإنترلوكين 4 (IL-4) على تعزيز استقطاب الخلايا البلعمية. وقد ثبت أن الخلايا الليمفاوية التائية التقليدية يمكنها تعزيز شفاء الأنسجة بشكل غير مباشر في الخلايا الليمفاوية التائية. نموذج الفأر من خلال تنظيم تمايز الخلايا الوحيدة والبلاعم.
وحيدة الخلية – خلية إصلاح متعددة القدرات
وفقًا لجهاز تحضير البلازما الغنية بالصفائح الدموية (PRP) المستخدم، قد تبرز الوحيدات أو لا توجد في زجاجة علاج البلازما الغنية بالصفائح الدموية (PRP).ولسوء الحظ، نادرا ما تتم مناقشة أدائهم وقدرتهم على التجديد في الأدبيات.ولذلك، يتم إيلاء القليل من الاهتمام للوحيدات في طريقة التحضير أو الصيغة النهائية.مجموعة الوحيدات غير متجانسة، تنشأ من الخلايا السلفية في نخاع العظم، ويتم نقلها إلى الأنسجة المحيطية من خلال مسار الخلايا الجذعية المكونة للدم وفقًا لتحفيز البيئة الدقيقة.أثناء التوازن والالتهاب، تترك الخلايا الوحيدة المنتشرة مجرى الدم ويتم تجنيدها في الأنسجة المصابة أو المتدهورة.يمكن أن تكون بمثابة خلايا بلاعمية (M Φ) أو خلايا سليفة.تمثل الخلايا الوحيدة والبلاعم والخلايا الجذعية النظام البلعمي أحادي النواة (MPS). السمة النموذجية لـ MPS هي مرونة نمط التعبير الجيني والتداخل الوظيفي بين أنواع الخلايا هذه.في الأنسجة المتدهورة، تقوم الخلايا البلعمية المقيمة، وعوامل النمو المؤثرة محليًا، والسيتوكينات المؤيدة للالتهابات، والخلايا المبرمجية أو النخرية والمنتجات الميكروبية ببدء الخلايا الوحيدة للتمايز إلى مجموعات خلايا MPS.لنفترض أنه عندما يتم حقن C-PRP الذي يحتوي على خلايا وحيدة عالية الإنتاجية في البيئة الدقيقة المحلية للمرض، فمن المرجح أن تتمايز الخلايا الوحيدة إلى M Φ لإحداث تغييرات كبيرة في الخلايا.
من خلية وحيدة إلى M Φ في عملية التحول، النمط الظاهري M Φ محدد.في السنوات العشر الأخيرة، تم تطوير نموذج يدمج M Φ. توصف آلية التنشيط المعقدة بأنها استقطاب حالتين متعارضتين: M Φ النمط الظاهري 1 (M Φ 1، التنشيط الكلاسيكي) والنمط الظاهري M Φ 2 (M Φ). 2، التنشيط البديل).يتميز MΦ1 بإفراز السيتوكينات الالتهابية (IFN-γ) وأكسيد النيتريك لإنتاج آلية فعالة لقتل مسببات الأمراض.M Φ ينتج النمط الظاهري أيضًا عامل نمو بطانة الأوعية الدموية (VEGF) وعامل نمو الخلايا الليفية (FGF).M Φ يتكون النمط الظاهري من خلايا مضادة للالتهابات ذات بلعمة عالية.M Φ 2 إنتاج مكونات المصفوفة خارج الخلية، وتولد الأوعية الدموية والكيميائيات، والإنترلوكين 10 (IL-10).بالإضافة إلى الدفاع عن مسببات الأمراض، يمكن لـ M Φ أيضًا تقليل الالتهاب وتعزيز إصلاح الأنسجة.من الجدير بالذكر أن M Φ 2 تم تقسيمها إلى M في المختبر Φ 2a، M Φ 2b و M Φ 2. يعتمد ذلك على التحفيز.من الصعب ترجمة هذه الأنواع الفرعية في الجسم الحي لأن الأنسجة قد تحتوي على مجموعات M Φ مختلطة.ومن المثير للاهتمام، أنه بناءً على الإشارات البيئية المحلية ومستويات IL-4، يمكن تحويل M Φ 1 المسببة للالتهابات لتعزيز الإصلاح M Φ 2. ومن هذه البيانات، من المعقول افتراض وجود تركيزات عالية من الخلايا الوحيدة ومستحضرات M Φ C-PRP. قد تساهم في إصلاح الأنسجة بشكل أفضل لأنها تتمتع بقدرات إصلاح الأنسجة المضادة للالتهابات ونقل إشارة الخلية.
تعريف مرتبك لجزء خلايا الدم البيضاء في PRP
يعتمد وجود خلايا الدم البيضاء في زجاجات العلاج بالبلازما الغنية بالصفائح الدموية (PRP) على جهاز تحضير البلازما الغنية بالصفائح الدموية (PRP) وقد يكون هناك اختلافات كبيرة.هناك العديد من الخلافات حول وجود الكريات البيض ومساهمتها في منتجات فرعية مختلفة من PRP (مثل PRGF وP-PRP وLP-PRP وLR-PRP وP-PRF وL-PRF). شملت التجارب ذات الشواهد (مستوى الأدلة 1) وثلاث دراسات مقارنة مستقبلية (مستوى الأدلة 2) 1055 مريضًا، مما يشير إلى أن LR-PRP وLP-PRP لهما سلامة مماثلة.وخلص المؤلف إلى أن التفاعل السلبي لـ PRP قد لا يكون مرتبطًا بشكل مباشر بتركيز خلايا الدم البيضاء.وفي دراسة أخرى، لم يغير LR-PRP الإنترلوكين الالتهابي (IL-1) في الركبة الفصالية β، وIL-6، وIL-8، وIL-17).تدعم هذه النتائج وجهة النظر القائلة بأن دور كريات الدم البيضاء في النشاط البيولوجي لـ PRP في الجسم الحي قد يأتي من الحديث المتبادل بين الصفائح الدموية وكريات الدم البيضاء.هذا التفاعل يمكن أن يعزز التخليق الحيوي لعوامل أخرى (مثل الأكسجين الشحمي)، والذي يمكن أن يعوض أو يعزز تراجع الالتهاب.بعد الإطلاق الأولي للجزيئات الالتهابية (حمض الأراكيدونيك، الليكوترين والبروستاجلاندين)، يتم إطلاق الأكسجين الشحمي A4 من الصفائح الدموية المنشطة لمنع تنشيط العدلات.في هذه البيئة يتحول النمط الظاهري M Φ من M Φ 1 إلى M Φ 2. بالإضافة إلى ذلك، هناك أدلة متزايدة على أن الخلايا وحيدة النواة المنتشرة يمكن أن تتمايز إلى مجموعة متنوعة من أنواع الخلايا غير البلعمية بسبب تعدد قدراتها.
سيؤثر نوع PRP على ثقافة MSC.بالمقارنة مع عينات PRP أو PPP النقية، يمكن أن يؤدي LR-PRP إلى تكاثر أعلى بكثير للخلايا الجذعية الصلبة المستمدة من النخاع العظمي (BMMSCs)، مع إطلاق أسرع ونشاط بيولوجي أفضل لـ PGF.كل هذه الخصائص تساعد على إضافة الخلايا الوحيدة إلى زجاجة العلاج بالبلازما الغنية بالصفائح الدموية (PRP) والتعرف على قدرتها على تعديل المناعة وإمكاناتها التمايزية.
التنظيم المناعي الخلقي والتكيفي لـ PRP
الوظيفة الفسيولوجية الأكثر شهرة للصفائح الدموية هي السيطرة على النزيف.تتراكم في موقع تلف الأنسجة والأوعية الدموية التالفة.تنجم هذه الأحداث عن التعبير عن الإنتغرينات والسيليكتينات التي تحفز التصاق الصفائح الدموية وتجمعها.تؤدي البطانة التالفة إلى تفاقم هذه العملية، كما أن الكولاجين المكشوف وغيره من بروتينات المصفوفة تحت البطانية تعزز التنشيط العميق للصفائح الدموية.في هذه الحالات، تم إثبات الدور الهام للتفاعل بين عامل فون ويلبراند (vWF) والبروتين السكري (GP)، وخاصة GP-Ib.بعد تنشيط الصفائح الدموية، تقوم الصفائح الدموية α-、 الكثيفة والليزوزومية وحبيبات T بتنظيم عملية خروج الخلايا وإطلاق محتوياتها في البيئة خارج الخلية.
جزيء التصاق الصفائح الدموية
من أجل فهم أفضل لدور PRP في الأنسجة الالتهابية والصفائح الدموية في الاستجابة المناعية، يجب أن نفهم كيف يمكن لمستقبلات سطح الصفائح الدموية المختلفة (integrins) وجزيئات التصاق الوصلات (JAM) والتفاعلات الخلوية أن تبدأ عمليات حرجة في المناعة الفطرية والتكيفية.
الإنتغرينات عبارة عن جزيئات تلتصق بسطح الخلية وتوجد في أنواع مختلفة من الخلايا ويتم التعبير عنها بكميات كبيرة على الصفائح الدموية.تتضمن التكاملات a5b1 وa6b1 وa2b1 LFA-2 و(GPIa/IIa) وaIIbb3 (GPIIb/IIIa).عادةً ما تكون موجودة في حالة ثابتة ومنخفضة التقارب.بعد التنشيط، يتحولون إلى حالة تقارب الارتباط العالي.للإنتيجرين وظائف مختلفة على الصفائح الدموية وتشارك في تفاعل الصفائح الدموية مع عدة أنواع من خلايا الدم البيضاء والخلايا البطانية والمصفوفة خارج الخلية.بالإضافة إلى ذلك، يتم التعبير عن مركب GP-Ib-V-IX على غشاء الصفائح الدموية وهو المستقبل الرئيسي للارتباط مع von vWF.يتوسط هذا التفاعل الاتصال الأولي بين الصفائح الدموية والهياكل تحت البطانية المكشوفة.يرتبط إنتغرين الصفائح الدموية ومركب GP بعمليات التهابية مختلفة ويلعبان دورًا مهمًا في تكوين مركب الصفائح الدموية والكريات البيض.على وجه التحديد، يعد الإنتغرين aIIbb3 ضروريًا لتكوين مركب مستقر من خلال الجمع بين الفيبرينوجين ومستقبل مستضد البلاعم 1 (Mac-1) على العدلات.
تعبر الصفائح الدموية والعدلات والخلايا البطانية الوعائية عن جزيئات محددة من التصاق الخلايا تسمى سيليكتين.في ظل الظروف الالتهابية، تعبر الصفائح الدموية عن P-selectin والعدلة L-selectin.بعد تنشيط الصفائح الدموية، قد يرتبط P-selectin بالربيطة PSGL-1 الموجودة على العدلات والخلايا الوحيدة.بالإضافة إلى ذلك، يؤدي ربط PSGL-1 إلى بدء تفاعل تسلسلي للإشارة داخل الخلايا، والذي ينشط العدلات من خلال العدلة إنتغرين Mac-1 والمستضد المرتبط بوظيفة الخلايا الليمفاوية 1 (LFA-1).يرتبط Mac-1 المنشط بـ GPIb أو GPIIb/IIIa على الصفائح الدموية من خلال الفيبرينوجين، وبالتالي استقرار التفاعل بين العدلات والصفائح الدموية.بالإضافة إلى ذلك، يمكن أن يتحد LFA-1 المنشط مع جزيء الالتصاق بين الخلايا للصفائح الدموية 2 لزيادة استقرار مركب العدلات والصفائح الدموية لتعزيز الالتصاق طويل الأمد مع الخلايا.
تلعب الصفائح الدموية والكريات البيض دورًا رئيسيًا في الاستجابات المناعية الفطرية والتكيفية
يمكن للجسم التعرف على الأجسام الغريبة والأنسجة المصابة في الأمراض الحادة أو المزمنة لبدء تفاعل التئام الجروح والمسار الالتهابي.تعمل أجهزة المناعة الفطرية والتكيفية على حماية المضيف من العدوى، وتلعب خلايا الدم البيضاء دورًا مهمًا في التداخل بين الجهازين.على وجه التحديد، تلعب الخلايا الوحيدة والبلاعم والعدلات والخلايا القاتلة الطبيعية دورًا رئيسيًا في الجهاز الفطري، بينما تلعب الخلايا الليمفاوية ومجموعاتها الفرعية دورًا مماثلاً في جهاز المناعة التكيفي.
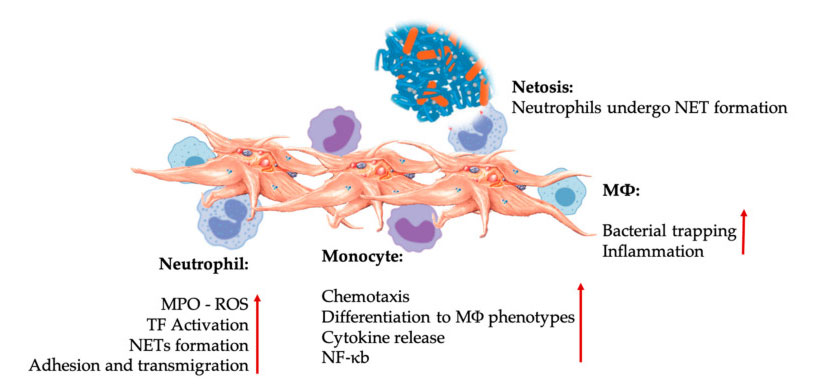
تفاعلات الصفائح الدموية والكريات البيض في تفاعلات الخلايا المناعية الفطرية.تتفاعل الصفائح الدموية مع العدلات والخلايا الوحيدة، وأخيرا مع M Φ تتفاعل، وتضبط وتزيد من وظائفها المستجيبة.تؤدي تفاعلات الصفائح الدموية مع كريات الدم البيضاء إلى الالتهاب من خلال آليات مختلفة، بما في ذلك التسمم بالنيتروجين.الاختصارات: MPO: الميلوبيروكسيديز، ROS: أنواع الأكسجين التفاعلية، TF: عامل الأنسجة، NET: مصيدة العدلات خارج الخلية، NF- κ B: العامل النووي kappa B، M Φ: البلاعم.
نظام المناعة الفطري
يتمثل دور الجهاز المناعي الفطري في تحديد الكائنات الحية الدقيقة الغازية أو شظايا الأنسجة بشكل غير محدد وتحفيز إزالتها.عندما تتحد هياكل جزيئية معينة تسمى مستقبلات التعرف على أنماط التعبير السطحي (PRRs) مع الأنماط الجزيئية المرتبطة بمسببات الأمراض والأنماط الجزيئية المرتبطة بالضرر، سيتم تنشيط الجهاز المناعي الفطري.هناك أنواع عديدة من مستقبلات PRR، بما في ذلك مستقبل Toll-like (TLR) وRIG-1 مثل مستقبل (RLR).يمكن لهذه المستقبلات تنشيط عامل النسخ الرئيسي kappa B (NF- κ B) كما أنها تنظم جوانب متعددة من الاستجابة المناعية الفطرية والتكيفية.ومن المثير للاهتمام، أن الصفائح الدموية تعبر أيضًا عن مجموعة متنوعة من جزيئات المستقبلات التنظيمية المناعية على سطحها والسيتوبلازم، مثل P-selectin، وبروتين الغشاء CD40 ligand (CD40L)، والسيتوكينات (مثل IL-1 β، وTGF- β)، وTLR الخاصة بالصفائح الدموية. ولذلك، يمكن للصفائح الدموية أن تتفاعل مع الخلايا المناعية المختلفة.
تفاعل الخلايا البيضاء والصفائح الدموية في المناعة الفطرية
عندما تدخل الصفائح الدموية أو تغزو تدفق الدم أو الأنسجة، فإن الصفائح الدموية هي إحدى الخلايا التي تكتشف إصابة بطانة الأوعية الدموية ومسببات الأمراض الميكروبية أولاً.تجميع الصفائح الدموية وتعزيز إطلاق منبهات الصفائح الدموية ADP، والثرومبين، وعامل فون ويلبراند (VWF)، مما يؤدي إلى تنشيط الصفائح الدموية والتعبير عن مستقبلات الصفائح الدموية الكيميائية C وCC وCXC وCX3C، مما يسبب الصفائح الدموية في الموقع المصاب أو الإصابة.
إن الجهاز المناعي الفطري محدد وراثيًا للكشف عن الغزاة، مثل الفيروسات والبكتيريا والطفيليات والسموم، أو جروح الأنسجة وجروحها.وهو نظام غير محدد، لأنه سيتم تحديد أي عامل ممرض على أنه أجنبي أو غير ذاتي وسيتم تحديد موقعه بسرعة.يعتمد الجهاز المناعي الفطري على مجموعة من البروتينات والخلايا البلعمية، التي تتعرف على الخصائص المحفوظة جيدًا لمسببات الأمراض وتقوم بتنشيط الاستجابة المناعية بسرعة للمساعدة في القضاء على الغزاة، حتى لو لم يتعرض المضيف لمسببات أمراض معينة من قبل.
تعد العدلات والوحيدات والخلايا الجذعية أكثر الخلايا المناعية الفطرية شيوعًا في الدم.تجنيدهم ضروري للاستجابة المناعية المبكرة الكافية.عندما يتم استخدام PRP في الطب التجديدي، فإن تفاعل الخلايا الصفائح الدموية البيضاء ينظم الالتهاب، والتئام الجروح وإصلاح الأنسجة.يحفز TLR-4 الموجود على الصفائح الدموية تفاعل الصفائح الدموية والعدلات، الذي ينظم ما يسمى انفجار أكسدة الكريات البيض عن طريق تنظيم إطلاق أنواع الأكسجين التفاعلية (ROS) والميلوبيروكسيديز (MPO) من العدلات.بالإضافة إلى ذلك، فإن التفاعل بين العدلات والصفائح الدموية وتحلل العدلات يؤدي إلى تكوين مصائد العدلات خارج الخلية (NETs).تتكون الشبكات من نواة العدلات ومحتويات أخرى داخل الخلايا من العدلات، والتي يمكنها التقاط البكتيريا وقتلها من خلال NETosis.يعد تكوين الشبكات آلية قتل أساسية للعدلات.
بعد تنشيط الصفائح الدموية، يمكن أن تهاجر الوحيدات إلى الأنسجة المريضة والتنكسية، حيث تقوم بأنشطة الالتصاق وتفرز جزيئات التهابية قد تغير الانجذاب الكيميائي وخصائص التحلل البروتيني.بالإضافة إلى ذلك، يمكن للصفائح الدموية أن تحفز تنشيط الوحيدات NF-κB لتنظيم وظيفة المستجيب للخلايا الوحيدة، والتي تعد الوسيط الرئيسي للاستجابة الالتهابية وتنشيط الخلايا المناعية وتمايزها.تعمل الصفائح الدموية أيضًا على تعزيز الانفجار التأكسدي الداخلي للخلايا الوحيدة لتعزيز تدمير مسببات الأمراض البلعمية.يتم التوسط في إطلاق MPO من خلال التفاعل المباشر بين الصفائح الدموية أحادية الخلية CD40L-MAC-1.ومن المثير للاهتمام، عندما يقوم P-selectin بتنشيط الصفائح الدموية في ظل حالات الأنسجة الالتهابية الحادة والمزمنة، فإن المركبات الكيميائية المشتقة من الصفائح الدموية PF4 و RANTES و IL-1 β و CXCL-12 يمكن أن تمنع موت الخلايا المبرمج التلقائي للخلايا الوحيدة، ولكنها تعزز تمايزها إلى بلاعم.
الجهاز المناعي التكيفي
بعد أن يتعرف الجهاز المناعي الفطري غير النوعي على الضرر الميكروبي أو الأنسجة، يتولى الجهاز المناعي التكيفي المحدد المسؤولية.تشتمل الأنظمة التكيفية على الخلايا الليمفاوية البائية المرتبطة بالمستضد (الخلايا البائية) والخلايا الليمفاوية التائية التقليدية (Treg) التي تنسق عملية إزالة مسببات الأمراض.يمكن تقسيم الخلايا التائية تقريبًا إلى خلايا تائية مساعدة (خلايا Th) وخلايا تائية سامة للخلايا (خلايا Tc، المعروفة أيضًا باسم الخلايا التائية القاتلة).وتنقسم الخلايا Th أيضًا إلى خلايا Th1 وTh2 وTh17، والتي لها وظائف رئيسية في الالتهاب.يمكن للخلايا Th أن تفرز السيتوكينات المسببة للالتهابات (مثل IFN- γ 、 TNF- β) والعديد من الإنترلوكينات (مثل IL-17). وهي فعالة بشكل خاص في الوقاية من الفيروسات داخل الخلايا والعدوى البكتيرية. تحفز الخلايا Th تكاثر وتمايز الخلايا المشاركة في هذه العملية. الاستجابة المناعية: الخلايا Tc هي خلايا مؤثرة يمكنها القضاء على الكائنات الحية الدقيقة والخلايا المستهدفة داخل الخلايا وخارجها.
ومن المثير للاهتمام، أن خلايا Th2 تنتج IL-4 وتؤثر على النمط الظاهري M Φ، والتجديد الموجه M Φ، بينما يتحول IFN- γ M Φ إلى النمط الظاهري الالتهابي M Φ 1، والذي يعتمد على جرعة ووقت السيتوكينات.بعد تنشيط IL-4، يحث M Φ 2 خلايا Treg على التمايز إلى خلايا Th2، ثم ينتج IL-4 إضافيًا (حلقة ردود فعل إيجابية).تقوم خلايا Th بتحويل M Φ ويتم توجيه النمط الظاهري إلى النمط الظاهري المتجدد استجابةً للعوامل البيولوجية ذات أصل الأنسجة.تعتمد هذه الآلية على الدليل على أن الخلايا التائية تلعب دورًا مهمًا في السيطرة على الالتهاب وإصلاح الأنسجة.
تفاعل خلايا الصفائح الدموية البيضاء في المناعة التكيفية
يستخدم الجهاز المناعي التكيفي مستقبلات خاصة بمستضد محدد ويتذكر مسببات الأمراض التي واجهها سابقًا، ويدمرها عندما يواجه المضيف لاحقًا.ومع ذلك، تطورت هذه الاستجابات المناعية التكيفية ببطء.كونياس وآخرون.ويظهر أن مكون الصفائح الدموية يساهم في إدراك المخاطر وإصلاح الأنسجة، وأن التفاعل بين الصفائح الدموية وخلايا الدم البيضاء يعزز تنشيط الاستجابة المناعية التكيفية.
أثناء الاستجابة المناعية التكيفية، تعمل الصفائح الدموية على تعزيز استجابات الخلايا الوحيدة والبلاعم من خلال نضوج الخلايا DC وNK، مما يؤدي إلى استجابات محددة للخلايا التائية والخلايا البائية.لذلك، تؤثر مكونات حبيبات الصفائح الدموية بشكل مباشر على المناعة التكيفية من خلال التعبير عن CD40L، وهو جزيء ضروري لتنظيم الاستجابة المناعية التكيفية.لا تلعب الصفائح الدموية من خلال CD40L دورًا في عرض المستضد فحسب، بل تؤثر أيضًا على تفاعل الخلايا التائية.ليو وآخرون.لقد وجد أن الصفائح الدموية تنظم استجابة خلايا CD4 T بطريقة معقدة.هذا التنظيم التفاضلي للمجموعات الفرعية لخلايا CD4 T يعني أن الصفائح الدموية تعزز خلايا CD4 T للاستجابة للمحفزات الالتهابية، وبالتالي إنتاج استجابات قوية مؤيدة للالتهابات ومضادة للالتهابات.
تنظم الصفائح الدموية أيضًا الاستجابة التكيفية للخلايا البائية لمسببات الأمراض الميكروبية.من المعروف أن CD40L الموجود على خلايا CD4 T المنشطة سيطلق CD40 للخلايا B، مما يوفر الإشارة الثانية المطلوبة لتنشيط الخلايا اللمفاوية B المعتمدة على الخلايا التائية، وتحويل النمط التخصيصي اللاحق، وتمايز الخلايا B وانتشارها.بشكل عام، تظهر النتائج بوضوح الوظائف المختلفة للصفائح الدموية في المناعة التكيفية، مما يشير إلى أن الصفائح الدموية تربط التفاعل بين الخلايا التائية والخلايا البائية من خلال CD40-CD40L، وبالتالي تعزيز استجابة الخلايا البائية المعتمدة على الخلايا التائية.بالإضافة إلى ذلك، الصفائح الدموية غنية بمستقبلات سطح الخلية، والتي يمكن أن تعزز تنشيط الصفائح الدموية وتطلق عددًا كبيرًا من الجزيئات النشطة الالتهابية والبيولوجية المخزنة في جزيئات الصفائح الدموية المختلفة، مما يؤثر على الاستجابة المناعية الفطرية والتكيفية.
توسيع دور السيروتونين المشتق من الصفائح الدموية في PRP
السيروتونين (5-هيدروكسيتريبتامين، 5-HT) له دور رئيسي واضح في الجهاز العصبي المركزي (CNS)، بما في ذلك تحمل الألم.تشير التقديرات إلى أن معظم 5-HT البشري يتم إنتاجه في الجهاز الهضمي ومن ثم من خلال الدورة الدموية، حيث يتم امتصاصه بواسطة الصفائح الدموية من خلال ناقل امتصاص السيروتونين ويتم تخزينه في جزيئات كثيفة بتركيزات عالية (65 مليمول / لتر).5-HT هو ناقل عصبي وهرمون معروف يساعد على تنظيم العمليات النفسية العصبية المختلفة في الجهاز العصبي المركزي (5-HT المركزي).ومع ذلك، فإن معظم 5-HT موجود خارج الجهاز العصبي المركزي (5-HT المحيطي)، ويشارك في تنظيم الوظائف البيولوجية الجهازية والخلوية لأنظمة أعضاء متعددة، بما في ذلك الأجهزة الوظيفية للقلب والأوعية الدموية والرئة والجهاز الهضمي والجهاز البولي التناسلي والصفائح الدموية.يحتوي 5-HT على استقلاب يعتمد على التركيز في مجموعة متنوعة من أنواع الخلايا، بما في ذلك الخلايا الشحمية والخلايا الظهارية وخلايا الدم البيضاء.يعد 5-HT المحيطي أيضًا مُعدِّلًا مناعيًا قويًا، والذي يمكن أن يحفز أو يمنع الالتهاب ويؤثر على الخلايا المناعية المختلفة من خلال مستقبل 5-HT المحدد (5HTR).
آلية Paracrine وautocrine من HT
يتم التوسط في نشاط 5-HT من خلال تفاعله مع 5HTRs، وهي فصيلة كبيرة مكونة من سبعة أعضاء (5-HT 1 – 7) وما لا يقل عن 14 نوعًا فرعيًا مختلفًا من المستقبلات، بما في ذلك العضو المكتشف مؤخرًا 5-HT 7، وأطرافه الطرفية و وظيفة في إدارة الألم.في عملية إزالة حبيبات الصفائح الدموية، تفرز الصفائح الدموية المنشطة عددًا كبيرًا من 5-HT المشتقة من الصفائح الدموية، والتي يمكن أن تعزز تقلص الأوعية الدموية وتحفز تنشيط الصفائح الدموية والخلايا الليمفاوية المجاورة من خلال التعبير عن 5-HTR على الخلايا البطانية وخلايا العضلات الملساء و الخلايا المناعية.باكالا وآخرون.تمت دراسة التأثير الانقسامي لـ 5-HT على الخلايا البطانية الوعائية، وتم تحديد إمكانية تعزيز نمو الأوعية الدموية التالفة عن طريق تحفيز تكوين الأوعية الدموية.إن كيفية تنظيم هذه العمليات ليست واضحة تمامًا، ولكنها قد تتضمن مسارات إشارة تفاضلية ثنائية الاتجاه في الدائرة الدقيقة للأنسجة لتنظيم وظائف الخلايا البطانية الوعائية وخلايا العضلات الملساء والخلايا الليفية والخلايا المناعية من خلال مستقبلات 5-HT محددة على هذه الخلايا. .تم وصف وظيفة الاستبداد للصفائح الدموية 5-HT بعد تنشيط الصفائح الدموية [REF].يعزز إطلاق 5-HT تنشيط الصفائح الدموية وتجنيد الصفائح الدموية المنتشرة، مما يؤدي إلى تنشيط تفاعلات الإشارة المتتالية والمؤثرات الأولية التي تدعم تفاعل الصفائح الدموية.
التأثير المناعي 5-HT
تظهر المزيد والمزيد من الأدلة أن السيروتونين يمكن أن يلعب دورًا في 5HTR المختلفة كمعدِّل مناعي.وفقًا لـ 5HTR المعبر عنه في الكريات البيض المختلفة المشاركة في التفاعل الالتهابي، يعمل 5-HT المشتق من الصفائح الدموية كمنظم مناعي في كل من أجهزة المناعة الفطرية والتكيفية.يمكن لـ 5-HT أن يحفز تكاثر Treg وينظم وظائف الخلايا البائية والخلايا القاتلة الطبيعية والعدلات عن طريق تجنيد DC وحيدات الخلية في الموقع الالتهابي.أظهرت الدراسات الحديثة أن 5-HT المشتق من الصفائح الدموية يمكنه تنظيم وظيفة الخلايا المناعية في ظل ظروف محددة.ولذلك، باستخدام C-PRP، فإن تركيز الصفائح الدموية أكبر من 1 × 10 6/ميكرولتر يمكن أن يساعد بشكل كبير في نقل تركيز 5-HT المشتق من الصفائح الدموية الكبيرة إلى الأنسجة.في البيئة الدقيقة التي تتميز بالمكونات الالتهابية، يمكن أن يتفاعل PRP مع العديد من الخلايا المناعية التي تلعب دورًا رئيسيًا في هذه الأمراض، مما قد يؤثر على النتائج السريرية.
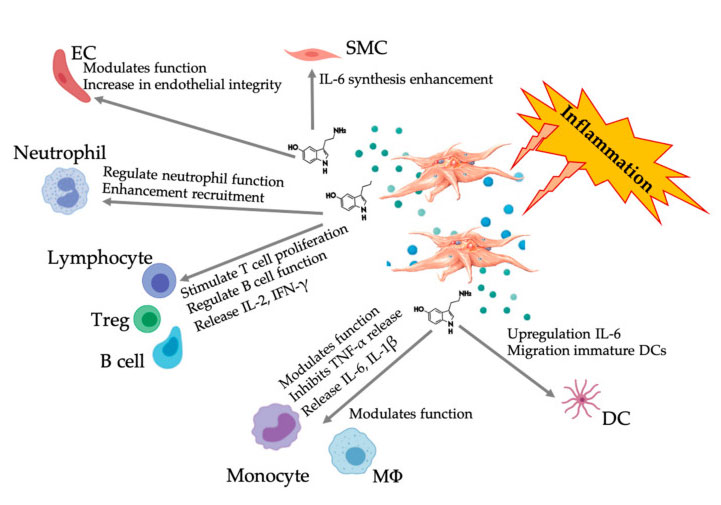
شكل يعرض استجابة 5-HT متعددة الأوجه بعد تنشيط الصفائح الدموية PRP الالتهابية.بعد تنشيط الصفائح الدموية، تطلق الصفائح الدموية حبيباتها، بما في ذلك 5-HT في حبيبات كثيفة، والتي لها مجموعة واسعة من التأثيرات التفاضلية على الخلايا المناعية المختلفة والخلايا البطانية وخلايا العضلات الملساء.الاختصارات: SMC: خلايا العضلات الملساء، EC: الخلايا البطانية، Treg: الخلايا الليمفاوية التائية التقليدية، M Φ : البلاعم، DC: الخلايا الجذعية، IL: إنترلوكين، IFN- γ : Interferon γ . معدلة ومقتبسة من Everts et al.و هال وآخرون.
تأثير مسكن للبلازما الغنية بالصفائح الدموية (PRP).
ستطلق الصفائح الدموية المنشطة العديد من الوسائط المؤيدة للالتهابات والمضادة للالتهابات، والتي لا تسبب الألم فحسب، بل تقلل أيضًا الالتهاب والألم.بمجرد تطبيقها، تعمل ديناميكيات الصفائح الدموية النموذجية لـ PRP على تغيير البيئة الدقيقة قبل إصلاح الأنسجة وتجديدها من خلال مجموعة متنوعة من المسارات المعقدة المتعلقة بالابتنائية والتقويض، وتكاثر الخلايا، والتمايز، وتنظيم الخلايا الجذعية.تؤدي خصائص البلازما الغنية بالصفائح الدموية إلى تطبيق البلازما الغنية بالصفائح الدموية في العديد من الحالات المرضية السريرية المرتبطة عادةً بالألم المزمن (مثل الإصابات الرياضية وأمراض العظام وأمراض العمود الفقري والجروح المزمنة المعقدة)، على الرغم من عدم تحديد الآلية الدقيقة بشكل كامل.
في عام 2008، إيفرتز وآخرون.إنها أول تجربة عشوائية محكومة للإبلاغ عن التأثير المسكن لمستحضر PRP، والذي يتم تحضيره من الطبقة البنية لمعدل ترسيب كرات الدم الحمراء الذاتي ويتم تنشيطه باستخدام الثرومبين الذاتي بعد جراحة الكتف.ولاحظوا انخفاضًا كبيرًا في درجات المقياس التناظري البصري، واستخدام المسكنات الأفيونية، وإعادة التأهيل بعد العملية الجراحية بشكل أكثر نجاحًا.من الجدير بالذكر أنها تعكس التأثير المسكن للصفائح الدموية المنشطة وتتكهن بآلية إطلاق الصفائح الدموية لـ 5-HT.باختصار، الصفائح الدموية تكون خاملة في البلازما الغنية بالصفائح الدموية الطازجة.بعد تنشيط الصفائح الدموية بشكل مباشر أو غير مباشر (عامل الأنسجة)، يتغير شكل الصفائح الدموية وتنتج كاذبة بما يكفي لتعزيز تراكم الصفائح الدموية.ثم يطلقون جزيئات ألفا وكثيفة داخل الخلايا.سيتم غزو الأنسجة المعالجة بـ PRP المنشط بواسطة PGF والسيتوكينات وغيرها من الجسيمات الحالة للصفائح الدموية.وبشكل أكثر تحديدًا، عندما تطلق الجزيئات الكثيفة محتوياتها، فإنها ستطلق كمية كبيرة من 5-HT الذي ينظم الألم.في C-PRP، يكون تركيز الصفائح الدموية أعلى بـ 5 إلى 7 مرات من تركيزه في الدم المحيطي.ولذلك، فإن إطلاق 5-HT من الصفائح الدموية يعد أمرًا فلكيًا.ومن المثير للاهتمام، سبروت وآخرون.ولاحظ التقرير أن الألم قد خف بشكل ملحوظ بعد الوخز بالإبر والكى، كما انخفض تركيز الصفائح الدموية المشتقة من 5-HT بشكل ملحوظ، ثم ارتفع مستوى البلازما 5-HT.
في المحيط، ستطلق الصفائح الدموية والخلايا البدينة والخلايا البطانية 5-HT داخليًا أثناء إصابة الأنسجة أو الصدمة الجراحية.ومن المثير للاهتمام، أنه تم اكتشاف مجموعة متنوعة من مستقبلات الخلايا العصبية 5-HT في المنطقة المحيطية، مما أكد أن 5-HT يمكن أن يتداخل مع انتقال مسبب للألم في المنطقة المحيطية.تظهر هذه الدراسات أن 5-HT يمكن أن يؤثر على انتقال مسبب الألم للأنسجة المحيطية من خلال مستقبلات 5-HT1 و5-HT2 و5-HT3 و5-HT4 و5-HT7.
يمثل نظام 5-HT نظامًا قويًا يمكنه تقليل وزيادة درجة الألم بعد التحفيز الضار.تم الإبلاغ عن التنظيم المركزي والمحيطي للإشارات المسببة للألم والتغيرات في نظام 5-HT في المرضى الذين يعانون من الألم المزمن.في السنوات الأخيرة، ركز عدد كبير من الدراسات على دور 5-HT ومستقبلاته في معالجة وتنظيم المعلومات الضارة، مما أدى إلى ظهور أدوية مثل مثبطات إعادة امتصاص السيروتونين الانتقائية (SSRI).يمنع هذا الدواء إعادة امتصاص السيروتونين إلى الخلايا العصبية قبل المشبكي بعد إطلاق السيروتونين.فهو يؤثر على مدة وشدة التواصل السيروتونين وهو علاج بديل للألم المزمن.هناك حاجة إلى مزيد من البحث السريري لفهم الآلية الجزيئية لتنظيم الألم 5-HT المشتق من PRP في الأمراض المزمنة والتنكسية.
يمكن الحصول على بيانات أخرى لحل التأثير المسكن المحتمل لـ PRP بعد اختبار النموذج الحيواني المسكن.تمثل الاستنتاجات الإحصائية المقارنة في هذه النماذج تحديًا لأن هذه الدراسات تحتوي على عدد كبير جدًا من المتغيرات.ومع ذلك، فقد تناولت بعض الدراسات السريرية التأثيرات المسببة للألم والمسكنة للبلازما الغنية بالصفائح الدموية.أظهرت العديد من الدراسات أن المرضى الذين يتلقون علاجًا لالتهاب الأوتار أو تمزقات الكفة المدورة لديهم القليل من الألم.في المقابل، أظهرت العديد من الدراسات الأخرى أن PRP يمكن أن يقلل أو حتى يزيل آلام المرضى الذين يعانون من تنكس الأوتار، والتهاب المفاصل العظمي، والتهاب اللفافة الأخمصية وأمراض القدم والكاحل الأخرى.تم تحديد تركيز الصفائح الدموية النهائي وتكوين الخلايا البيولوجية كخصائص رئيسية للبلازما الغنية بالصفائح الدموية (PRP)، والتي تساعد على ملاحظة التأثير المسكن الثابت بعد تطبيق البلازما الغنية بالصفائح الدموية (PRP).تشمل المتغيرات الأخرى طريقة توصيل PRP، وتكنولوجيا التطبيق، وبروتوكول تنشيط الصفائح الدموية، ومستوى النشاط البيولوجي لـ PGF والسيتوكينات المنطلقة، ونوع الأنسجة لتطبيق PRP ونوع الإصابة.
من الجدير بالذكر أن كوفلر نجح في حل إمكانية استخدام البلازما الغنية بالصفائح الدموية (PRP) في تخفيف الألم لدى المرضى الذين يعانون من آلام الأعصاب المزمنة الخفيفة إلى الشديدة، الثانوية للعصب غير المتجدد التالف.الغرض من هذه الدراسة هو معرفة ما إذا كان من الممكن تقليل آلام الأعصاب أو تخفيفها بسبب تعزيز PRP لتجديد محور عصبي وإعادة تعصيب العصب المستهدف.والمثير للدهشة أنه من بين المرضى الذين يتلقون العلاج، لا يزال ألم الاعتلال العصبي يتم التخلص منه أو تخفيفه بعد ست سنوات على الأقل من الجراحة.وبالإضافة إلى ذلك، بدأ جميع المرضى في تخفيف الألم في غضون ثلاثة أسابيع بعد تطبيق PRP.
في الآونة الأخيرة، لوحظت تأثيرات مسكنة مماثلة للبلازما الغنية بالصفائح الدموية (PRP) في مجال العناية بالجروح والعناية بالبشرة بعد العملية الجراحية.ومن المثير للاهتمام أن المؤلفين أبلغوا عن الجوانب الفسيولوجية لألم الجرح المرتبط بإصابة الأوعية الدموية ونقص الأكسجة في أنسجة الجلد.وناقشوا أيضًا أهمية تكوين الأوعية الدموية في تحسين الأوكسجين وتوصيل المغذيات.وأظهرت دراستهم أنه بالمقارنة مع المجموعة الضابطة، كان المرضى الذين يتلقون العلاج بالبلازما الغنية بالصفائح الدموية يعانون من ألم أقل وزيادة كبيرة في تكوين الأوعية الدموية.أخيرًا، أجرى جوهال وزملاؤه مراجعة منهجية وتحليلًا تلويًا وخلصوا إلى أن البلازما الغنية بالصفائح الدموية يمكن أن تقلل الألم بعد استخدام البلازما الغنية بالصفائح الدموية في مؤشرات العظام، خاصة في المرضى الذين يتلقون التهاب اللقيمة الخارجي وعلاج الزراعة العضوية في الركبة.لسوء الحظ، لم تحدد هذه الدراسة تأثيرات خلايا الدم البيضاء، أو تركيز الصفائح الدموية، أو استخدام منشطات الصفائح الدموية الخارجية، لأن هذه المتغيرات من شأنها أن تؤثر على الفعالية الشاملة لـ PRP.إن التركيز الأمثل للصفائح الدموية PRP لتحقيق أقصى قدر من تخفيف الألم غير واضح.في نموذج الفئران لالتهاب الأوتار، كان تركيز الصفائح الدموية 1.0 × 10 6 / μ عند L، يمكن تخفيف الألم تمامًا، في حين يتم تقليل تخفيف الألم الناجم عن PRP بنصف تركيز الصفائح الدموية بشكل كبير.لذلك، نحن نشجع على إجراء المزيد من الدراسات السريرية للتحقيق في التأثيرات المسكنة لمستحضرات البلازما الغنية بالصفائح الدموية (PRP) المختلفة.
PRP وتأثير الأوعية الدموية
تسمح مستحضرات C-PRP في الطب التجديدي الدقيق بتوصيل الجزيئات الحيوية الصادرة عن طريق تركيزات عالية من الصفائح الدموية التي يتم تنشيطها في مواقع الأنسجة المستهدفة.لذلك، تم بدء مجموعة متنوعة من التفاعلات المتتالية، والتي تساهم في تنظيم المناعة في الموقع، والعملية الالتهابية وتولد الأوعية لتعزيز الشفاء وإصلاح الأنسجة.
تكوين الأوعية الدموية هو عملية ديناميكية متعددة الخطوات تتضمن الإنبات والأوعية الدقيقة للأنسجة من الأوعية الدموية الموجودة مسبقًا.لقد تقدم تكوين الأوعية الدموية بسبب مجموعة متنوعة من الآليات البيولوجية، بما في ذلك هجرة الخلايا البطانية، والانتشار، والتمايز والانقسام.هذه العمليات الخلوية هي متطلبات أساسية لتشكيل أوعية دموية جديدة.فهي ضرورية لنمو الأوعية الدموية الموجودة مسبقًا لاستعادة تدفق الدم ودعم النشاط الأيضي العالي لإصلاح الأنسجة وتجديد الأنسجة.تسمح هذه الأوعية الدموية الجديدة بتوصيل الأكسجين والمواد المغذية، وإزالة المنتجات الثانوية من الأنسجة المعالجة.
يتم تنظيم نشاط تكوين الأوعية عن طريق تحفيز العامل الوعائي VEGF والعوامل المضادة لتولد الأوعية (مثل الأنجيوستاتين والثرومبوسبوندين -1 [TSP-1]).في البيئة المكروية المريضة والمتدهورة (بما في ذلك انخفاض توتر الأكسجين، وانخفاض الرقم الهيدروجيني وارتفاع مستوى حمض اللاكتيك)، ستعمل العوامل الوعائية المحلية على استعادة نشاط تكوين الأوعية الدموية.
يمكن للعديد من الوسائط القابلة للذوبان في الصفائح الدموية، مثل FGF الأساسي وTGF-β وVEGF تحفيز الخلايا البطانية لإنتاج أوعية دموية جديدة.أبلغ Landsdown وFortier عن نتائج مختلفة تتعلق بتركيبة PRP، بما في ذلك المصادر داخل الصفائح الدموية للعديد من منظمات تكوين الأوعية الدموية.بالإضافة إلى ذلك، خلصوا إلى أن زيادة تكوين الأوعية الدموية يساهم في شفاء مرض MSK في المناطق التي تعاني من ضعف الأوعية الدموية، مثل تمزق الغضروف المفصلي، وإصابة الأوتار وغيرها من المناطق التي تعاني من ضعف الأوعية الدموية.
تعزيز وخصائص الصفائح الدموية المضادة للتولد الوعائي
في العقود القليلة الماضية، أثبتت الدراسات المنشورة أن الصفائح الدموية تلعب دورًا رئيسيًا في الإرقاء الأولي، وتكوين الجلطة، وعامل النمو وإطلاق السيتوكينات، وتنظيم تكوين الأوعية الدموية كجزء من عملية إصلاح الأنسجة.ومن المفارقة أن PRP α - تحتوي الحبيبات على ترسانة من عوامل النمو المؤيدة لتكوين الأوعية، والبروتينات المضادة لتكوين الأوعية الدموية والسيتوكينات (مثل PF4، ومثبط منشط البلازمينوجين -1 وTSP-1)، وتستهدف إطلاق عوامل محددة تلعب دورًا. .دور في تكوين الأوعية الدموية.لذلك، يمكن تحديد دور PRP في التحكم في تنظيم تكوين الأوعية من خلال تنشيط مستقبلات معينة على سطح الخلية، TGF-β يبدأ التفاعلات المؤيدة لتولد الأوعية الدموية والمضادة لتولد الأوعية.تم تأكيد قدرة الصفائح الدموية على ممارسة مسار تكوين الأوعية الدموية في تكوين الأوعية الدموية المرضية وتولد الأوعية الدموية للورم.
عامل النمو الوعائي المشتق من الصفائح الدموية وعامل النمو المضاد للتولد الوعائي، المشتق من α- والجزيئات الكثيفة واللاصقة.والأهم من ذلك، أنه من المقبول عمومًا أن التأثير الإجمالي للصفائح الدموية على تكوين الأوعية الدموية يكون مؤيدًا ومحفزًا للتولد الوعائي.ومن المتوقع أن يتحكم علاج PRP في تحفيز تكوين الأوعية الدموية، مما سيساهم في التأثير العلاجي للعديد من الأمراض، مثل التئام الجروح وإصلاح الأنسجة.يمكن أن يؤدي إعطاء PRP، وبشكل أكثر تحديدًا إعطاء PGF عالي التركيز وسيتوكينات الصفائح الدموية الأخرى، إلى تحفيز تكوين الأوعية الدموية وتولد الأوعية الدموية وتولد الشرايين، لأن العامل المشتق من الخلايا اللحمية 1a يرتبط بمستقبل CXCR4 على الخلايا السلفية البطانية.بيل وآخرون.يقترح أن PRP يزيد من الأوعية الدموية الإقفارية، والتي قد تكون ناجمة عن تحفيز تكوين الأوعية الدموية، وتولد الأوعية الدموية، وتولد الشرايين.في نموذجهم المختبري، تم تحفيز تكاثر الخلايا البطانية وتكوين الشعيرات الدموية بواسطة عدد كبير من PDGs المختلفة، والتي كان VEGF هو المحفز الوعائي الرئيسي فيها.هناك عامل مهم وأساسي آخر لاستعادة مسار تكوين الأوعية وهو التآزر بين PGFs المتعددة.ريتشاردسون وآخرون.لقد ثبت أن النشاط التآزري لعامل النمو المشتق من الصفائح الدموية العامل الوعائي-bb (PDGF-BB) وVEGF أدى إلى التكوين السريع لشبكة الأوعية الدموية الناضجة مقارنة بنشاط عامل النمو الفردي.تم تأكيد التأثير المشترك لهذه العوامل مؤخرًا في دراسة أجريت على تعزيز الدورة الدموية الدماغية لدى الفئران التي تعاني من نقص تدفق الدم على المدى الطويل.
والأهم من ذلك، قامت دراسة في المختبر بقياس التأثير التكاثري للخلايا البطانية للوريد السري البشري وتركيزات الصفائح الدموية المختلفة على اختيار جهاز تحضير PRP واستراتيجية جرعة الصفائح الدموية، وأظهرت النتائج أن جرعة الصفائح الدموية المثالية كانت 1.5 × 10 6 صفائح / μ 50. لتعزيز تكوين الأوعية الدموية.قد يؤدي تركيز الصفائح الدموية المرتفع جدًا إلى تثبيط عملية تكوين الأوعية الدموية، وبالتالي يكون التأثير ضعيفًا.
شيخوخة الخلايا والشيخوخة وPRP
يمكن أن يحدث شيخوخة الخلايا عن طريق المحفزات المختلفة.هذه هي العملية التي تتوقف فيها الخلايا عن الانقسام وتخضع لتغييرات ظاهرية فريدة لمنع النمو غير المقيد للخلايا التالفة، وهو ما يلعب دورًا مهمًا في الوقاية من السرطان.في عملية الشيخوخة الفسيولوجية، ستعمل شيخوخة تكرار الخلايا أيضًا على تعزيز شيخوخة الخلايا، وستنخفض قدرة الخلايا الجذعية السرطانية على التجدد.
آثار الشيخوخة وشيخوخة الخلايا
في الجسم الحي، العديد من أنواع الخلايا سوف تتقدم في السن وتتراكم في الأنسجة المختلفة أثناء الشيخوخة، ومن بينها عدد كبير من الخلايا الهرمة.يبدو أن تراكم خلايا الشيخوخة يزداد مع تقدم العمر أو تلف الجهاز المناعي أو تلف الأنسجة أو العوامل المرتبطة بالتوتر.تم تحديد آلية الشيخوخة الخلوية باعتبارها العامل الممرض للأمراض المرتبطة بالعمر، مثل هشاشة العظام وهشاشة العظام وتنكس القرص الفقري.مجموعة متنوعة من المحفزات سوف تؤدي إلى تفاقم شيخوخة الخلايا.رداً على ذلك، فإن النمط الظاهري الإفرازي المرتبط بالشيخوخة (SASP) سوف يفرز تركيزات عالية من الخلايا البروتينية والسيتوكينات.يرتبط هذا النمط الظاهري الخاص بخلايا الشيخوخة، حيث تفرز مستويات عالية من السيتوكينات الالتهابية (مثل IL-1، IL-6، IL-8)، وعوامل النمو (مثل TGF- β، HGF، VEGF، PDGF)، MMP، وكاثيبسين.بالمقارنة مع الشباب، ثبت أن SAPS يزداد مع تقدم العمر، لأنه يتم تدمير عملية الحالة المستقرة، مما يؤدي إلى شيخوخة الخلايا وانخفاض القدرة على التجدد.على وجه التحديد، في أمراض المفاصل وأمراض العضلات والهيكل العظمي.في هذا الصدد، تعتبر الشيخوخة المناعية بمثابة تغير كبير في طيف إفراز الخلايا المناعية، مما يشير إلى أن تركيز TNF-a و/أو IL-6 و/أو Il-1b يزداد، مما يؤدي إلى التهاب مزمن منخفض الدرجة.ومن الجدير بالذكر أن خلل الخلايا الجذعية يرتبط أيضًا بآليات مستقلة غير خلوية، مثل الخلايا المتقدمة في السن، وخاصة إنتاج العوامل المؤيدة للالتهابات والمضادة للتجدد من خلال SASP.
على العكس من ذلك، يمكن لـ SASP أيضًا تحفيز مرونة الخلايا وإعادة برمجة الخلايا المجاورة.بالإضافة إلى ذلك، يمكن لـ SASP تنظيم الاتصال مع مختلف وسطاء المناعة وتنشيط الخلايا المناعية لتعزيز إزالة الخلايا الهرمة.إن فهم دور ووظيفة الخلايا المتقدمة في السن سيساهم في شفاء وإعادة تشكيل أنسجة عضلات MSK والجروح المزمنة.
ومن الجدير بالذكر أن ريتاكا وآخرون.تم إجراء دراسة موسعة، وتم اكتشاف الدور الرئيسي والمفيد لـ SASP في تعزيز مرونة الخلايا وتجديد الأنسجة، وتم تقديم مفهوم تقديم العلاج العابر للخلايا المتقدمة في السن.وذكروا بحذر أن الشيخوخة هي في الأساس عملية مفيدة وتجديدية.
شيخوخة الخلايا وإمكانات PRP
ومع انخفاض عدد الخلايا الجذعية، فإن الشيخوخة سوف تؤثر على أداء الخلايا الجذعية.وبالمثل، عند البشر، تتناقص أيضًا خصائص الخلايا الجذعية (مثل الجفاف والتكاثر والتمايز) مع تقدم العمر.أفاد وانغ ونيرمالا أن الشيخوخة من شأنها أن تقلل من خصائص الخلايا الجذعية للخلايا الوترية وعدد مستقبلات عامل النمو.أظهرت دراسة أجريت على الحيوانات أن تركيز PDGF في الخيول الصغيرة كان مرتفعًا.وخلصوا إلى أن الزيادة في عدد مستقبلات GF وعدد GF لدى الشباب قد يكون لها استجابة خلوية أفضل لعلاج PRP مقارنة بالأفراد الأكبر سنا لدى الشباب.تكشف هذه النتائج لماذا قد يكون علاج PRP أقل فعالية أو حتى غير فعال في المرضى المسنين الذين لديهم عدد أقل من الخلايا الجذعية و"نوعية رديئة".لقد ثبت أن عملية شيخوخة الغضروف تنعكس وتزداد فترة راحة الخلايا الغضروفية بعد حقن البلازما الغنية بالصفائح الدموية.جيا وآخرون.يتم استخدامه لدراسة الخلايا الليفية الجلدية في الفئران في التصوير الفوتوغرافي في المختبر، مع أو بدون علاج PRP، لتوضيح آلية مقاومة PGF في هذا النموذج.أظهرت مجموعة PRP تأثيرًا مباشرًا على المصفوفة خارج الخلية، وزيادة الكولاجين من النوع الأول وتقليل تخليق البروتينات المعدنية، مما يشير إلى أن PRP يمكنه مقاومة شيخوخة الخلايا، وكذلك في مرض MSK التنكسية.
وفي دراسة أخرى، تم استخدام PRP لجمع الخلايا الجذعية لنخاع العظم من الفئران المسنة.لقد تم تحديد أن PRP يمكنه استعادة مجموعة متنوعة من وظائف الخلايا الجذعية من الشيخوخة، مثل تكاثر الخلايا وتكوين المستعمرات، وإعادة بناء العلامات المتعلقة بشيخوخة الخلايا.
في الآونة الأخيرة، قام أوبرلوهر وزملاؤه بدراسة مكثفة لدور شيخوخة الخلايا في إضعاف تجديد العضلات، وقاموا بتقييم البلازما الغنية بالصفائح الدموية (PRP) والبلازما الفقيرة بالصفائح الدموية (PPP) كخيارات علاج بيولوجي لإصلاح العضلات الهيكلية.لقد تصوروا أن علاج PRP أو PPP لإصلاح العضلات الهيكلية سيعتمد على عوامل بيولوجية مخصصة لعلامات الخلايا المحددة لـ SASP وعوامل أخرى تؤدي إلى تطور التليف.
من المعقول الاعتقاد أنه قبل تطبيق PRP، يمكن لشيخوخة الخلايا المستهدفة تحسين خصائص تجديد فعالية العلاج البيولوجي عن طريق تقليل عوامل SASP المحلية.لقد تم اقتراح أن هناك خيارًا آخر لتحسين نتائج علاج PRP و PPP لتجديد العضلات الهيكلية وهو إزالة خلايا الشيخوخة بشكل انتقائي مع زبالين الشيخوخة.ليس هناك شك في أن نتائج الأبحاث الحديثة حول تأثير PRP على شيخوخة الخلايا وشيخوخة الخلايا رائعة، لكنها لا تزال في المرحلة الأولية.ولذلك، فمن غير المعقول تقديم أي اقتراحات في هذا الوقت.
(محتويات هذه المقالة أعيد طباعتها، ونحن لا نقدم أي ضمان صريح أو ضمني لدقة أو موثوقية أو اكتمال المحتويات الواردة في هذه المقالة، ولسنا مسؤولين عن آراء هذه المقالة، يرجى تفهم ذلك.)
وقت النشر: 01 مارس 2023